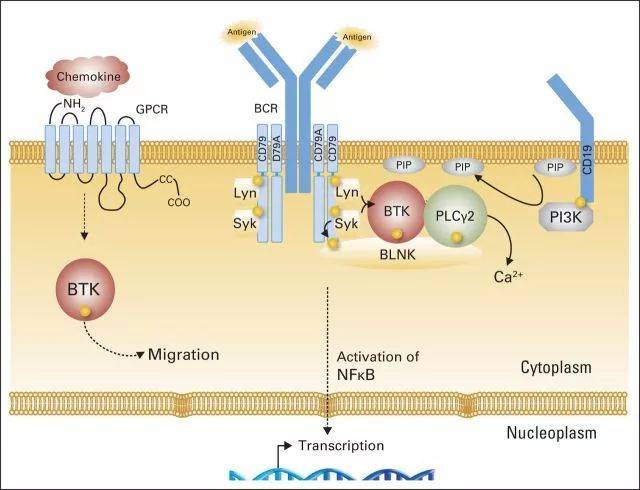
本报讯(记者袁璐)中国新药研发迎来重大里程碑。今天上午,百济神州公司宣布,其自主研发的BTK抑制剂泽布替尼通过美国食品药品监督管理局(FDA)加速批准,用于治疗既往接受过至少一项疗法的套细胞淋巴瘤(MCL)患者。这标志着,泽布替尼成为迄今为止第一款完全由中国企业自主研发、在FDA获准上市的抗癌新药,实现中国原研新药出海“零的突破”,改写了中国抗癌药“只进不出”的尴尬历史。
记者了解到,在目前已知的淋巴瘤70多个亚型中,套细胞淋巴瘤侵袭性较强,中位生存期仅为三至四年。多数患者在确诊时已处于疾病晚期,面临着治疗手段有限、预后不良的困境。而泽布替尼则是一款新型强效BTK抑制剂,目前正作为单药或与其他疗法联合用药,在多种淋巴瘤治疗中开展临床试验。数据显示,在针对套细胞淋巴瘤的临床试验中,84%以上接受泽布替尼治疗的患者达到了总体缓解。
长期以来,在我国上市的抗癌原研药主要依赖进口,而从本土出口海外的药品则多为原料药或仿制药,总体对全球医药创新体系的贡献相对较小。近年,我国医药行业加快转型升级,尤其在药改、医改的利好政策驱动下,制药业兴起创新浪潮,大批科学家归国投入新药研发,为医药产业从仿制转向创新、从本土走向全球,注入了可持续发展的活力。
泽布替尼诞生于北京昌平的百济神州研发中心。百济神州方面透露,泽布替尼获得FDA批准是基于两项临床试验的有效性数据,其中关键性2期临床研究由北京大学肿瘤医院牵头开展。“近年来,我国淋巴瘤的临床治疗和药物研发步入快速发展的时期。曾经,我们只能期待国外的新药进入中国,如今情况发生了极大改变。”北京大学肿瘤医院淋巴瘤科主任朱军表示,本土自主研发的新药首次在FDA获准上市,代表着我国的创新能力和研究水平得到国际上的肯定,为世界提供中国的治疗方案。
记者了解到,百济神州已于2018年8月和10月,向中国国家药品监督管理局(NMPA)递交了泽布替尼针对治疗复发或难治性套细胞淋巴瘤(MCL)与复发难治性慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)的新药上市申请,并均被纳入优先审评通道,有望早日惠及我国本土患者。在国内获批后,泽布替尼将在百济神州位于苏州桑田岛工业园区的小分子药物生产基地进行商业化生产。
(编辑:鑫果)







 镜头下的“电疗神坛”:科治好骗局十年未凉,老人带娃入局背后的情感围猎
镜头下的“电疗神坛”:科治好骗局十年未凉,老人带娃入局背后的情感围猎 假洋膏药年销过亿元,平台监管不能失灵
假洋膏药年销过亿元,平台监管不能失灵 AI投资陷阱与维权难,企业如何防范技术合作骗局
AI投资陷阱与维权难,企业如何防范技术合作骗局 “护眼台灯”乱象调查
“护眼台灯”乱象调查